Článek
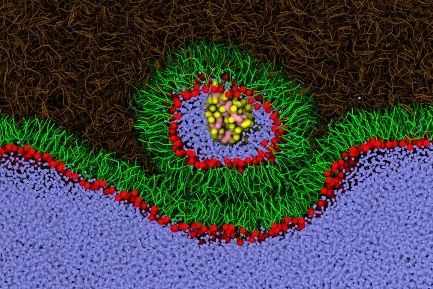
Metoda využívající vlastnosti takzvané fluorescenční superrozlišovací mikroskopie (bSOFI) umožňuje sledovat procesy v buňkách a na jejich povrchu v rozlišení okolo 25 nanometrů, tedy miliardtin metru. To je desetkrát ostřejší obraz než v případě standardní mikroskopie, jak demonstruje úvodní obrázek.
Je to, jako bychom na satelitní fotografii lesa dokázali rozeznat jednotlivé stromy. Začínáme pracovat na uživatelsky příjemném softwaru, aby se mohl hojněji využívat.
Tato metoda se zaměřuje na hustotu jednotlivých molekul v konkrétních lokalitách. Vědci uvedli, že v určitých aspektech posouvá dosavadní hranice bSOFI, za niž byla v roce 2014 udělena Nobelova cena za chemii. Tehdy byli za vývoj mikroskopu s velkým rozlišením oceněni Američané Eric Betzig a William Moerner s Němcem Stefanem Hellem.
„Zjednodušeně řečeno je to, jako bychom na satelitní fotografii lesa dokázali konečně rozeznat jednotlivé stromy. Samotná metoda je dosti složitá, ale v publikované práci ji dáváme volně k dispozici a začínáme pracovat na uživatelsky příjemném softwaru, aby se mohla hojněji využívat. Možnosti jejího využití jsou totiž široké,“ konstatoval Cebecauer.
Porozumění bílým krvinkám
Novou metodu hodlá Cebecauer jakožto biochemik využít ve výzkumu imunitního systému. „Zajímá nás funkce lymfocytů a obecně lidské imunity,“ vysvětlil.
„Molekuly na povrchu lymfocytů, například bílých krvinek, nejsou rozprostřeny náhodně. Objevujeme je ve shlucích. Ale proč? Sledováním ve vyšším rozlišení můžeme zjistit spoustu nových informací o organizaci molekul, které ovlivňují různé důležité procesy včetně funkce nebo nefunkce obranného systému našeho těla,“ řekl.
Ve většině případů se lidská onemocnění vysvětlují ztrátou funkce důležité látky v našem těle. „V mnoha případech však toto zdůvodnění selhává. Proto se nabízejí jiné teorie a hypotézy, například narušení přesného seskupení konkrétních látek. Jenže o přesné lokalizaci látek v našem těle se toho ví zatím stále málo,“ pokračoval Cebecauer.
Důvodem je podle něj malá dostupnost vhodných metod pro studium molekul v buňkách s přesností v řádu nanometrů. I proto se jeho skupina zaměřuje na studium přesné lokalizace důležitých molekul v našem těle, konkrétně v imunitních a neurálních buňkách.
„Snažíme se popsat vliv změn umístění konkrétních látek na funkci imunitního systému a rozluštit tak důvody nemocí, o kterých zatím moc nevíme,“ shrnul.
Zkoumání interakcí imunitních buněk s okolím na nejelementárnější úrovni může vysvětlit, jak spolu celý složitý systém v našich tělech komunikuje.
„Může teoreticky pomoci pochopit zákonitosti vzniku a průběhu autoimunitních onemocnění či naopak nedostatečné imunitní reakce včetně rakoviny. Zajímá nás vliv faktorů moderní společnosti, jako je například zátěžový stres, na rozvoj psychických potíží. I u Parkinsonovy a Alzheimerovy choroby postrádáme vysvětlení jejich vzniku v ranějších stadiích života. Naší metodou by mělo být možné rozeznat změny uspořádání kritických látek při vývoji nemocí, lépe je klasifikovat a sledovat, jak reagují na různé změny způsobené stárnutím organismu či zhoršujícím se životním prostředím,“ uzavřel.
Čeští odborníci na tom spolupracovali s kolegy ze Švýcarského federálního technologického institutu v Lausanne (EPFL). O objevu informoval i vědecký časopis Nature Communications.